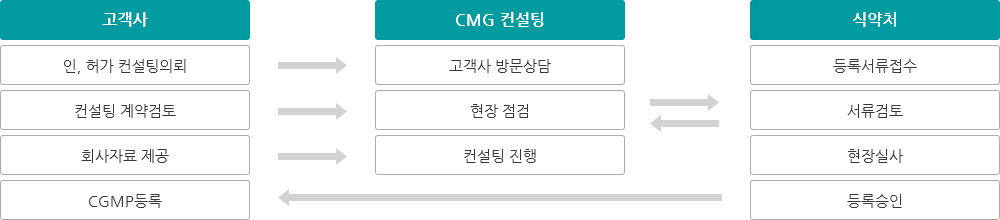
식약처CGMP에서 요구하고 있는 우수화장품 제조 및 품질관리기준(CGMP)에 부합하는 제조소의 Concept Design, 4대기준서, 설비요구사항, 품질시스템 구축 등에 대한 컨설팅 서비스를 제공합니다.
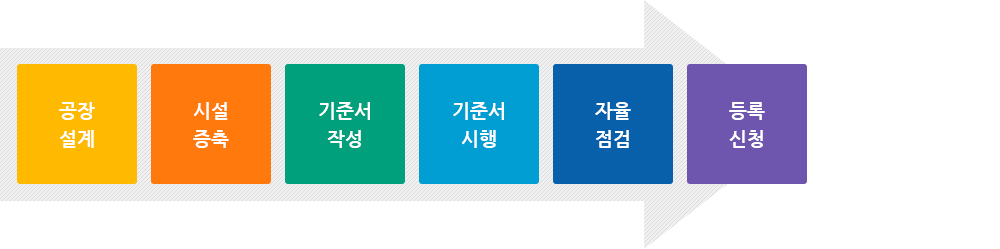
컨설팅 절차
컨설팅 개요
컨설팅 ROAD MAP
| Objective |
Key deliverables |
Detail Action Plan |
1 |
2 |
3 |
4 |
5 |
6 |
| Project Preparation |
TFT 팀 구성 |
업체의 컨설팅 업무 참여인원 지정 |
|
|
|
|
|
|
| Kick-off 미팅 |
CMG컨설팅과 고객사간의 일정확인 |
|
|
|
|
|
|
| 프로젝트 최종준비 |
생산현장 방문 및 상황 점검 |
|
|
|
|
|
|
| Analysis of Current system |
시스템 자료분석 |
고객사의 시스템 및 문서 확인 |
|
|
|
|
|
|
| 현장 확인 |
제조소 및 설비상황 점검 |
|
|
|
|
|
|
| GAP Analysis |
Audit |
시스템의 GAP분석, 개선사항 확정 |
|
|
|
|
|
|
| Output Design |
규정 및 절차서, 기록물에 대한 디자인 |
|
|
|
|
|
|
| Education |
Education |
관료규정 및 제반 사항에 대한 지속적인 교육 |
|
|
|
|
|
|
| Drafting |
Drafting |
관련 문서 작성 |
|
|
|
|
|
|
| Presentation |
고객사와의 미팅 및 보완 개선사항 점검 |
|
|
|
|
|
|
| Completion of Output |
수정/보완점이 반영된 최종 개정본 작성 |
|
|
|
|
|
|
| Final output |
Presentation |
최종 시스템, 문서 소개 및 설명 |
|
|
|
|
|
|
| Review |
최종문서에 대한 리뷰 및 의견 반영 |
|
|
|
|
|
|
| Implementation |
적용개시 |
완성된 시스템의 현장적용 |
|
|
|
|
|
|
| 적용 점검 및 검토 |
적용된 시스템의 유지상태확인 및 개선 |
|
|
|
|
|
|
| Final Check |
내부심사 |
내부심사 및 보완 |
|
|
|
|
|
|
| 개선 및 신청 |
내부심사에 따른 개선 및 등록심사 신청 |
|
|
|
|
|
|
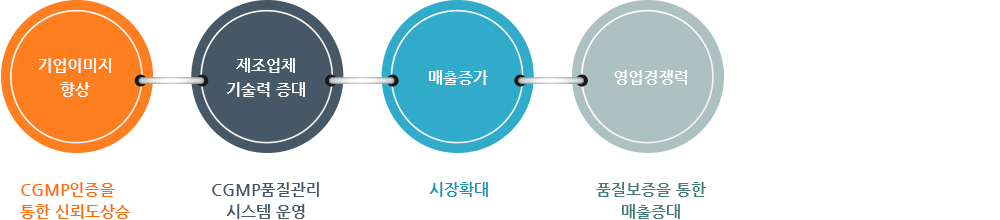
기대효과